Le rapport sur les essais cliniques de Veeva MedTech signale une occasion importante d'améliorer la distribution et la qualité des données
83 % utilisent les e-mails, les portails et le papier pour échanger des informations avec les partenaires de l'étude, ce qui ralentit l'exécution de l'étude et augmente le risque de non-conformité.
BARCELONE, Espagne, 20 avril 2023 /PRNewswire/ -- Veeva Systems (NYSE: VEEV) a publié aujourd'hui son tout premier rapport sur les tendances mondiales concernant les essais cliniques réalisés par des medtech. Selon le rapport de référence clinique 2023 de Veeva MedTech, la saisie des données à temps et la qualité des données sont les principaux défis des entreprises de medtech lorsqu'elles travaillent avec des sites de recherche clinique. Cela peut retarder les essais et accroître les risques en matière de conformité ; c'est pourquoi améliorer la collaboration avec les sites d'étude est une priorité essentielle pour une livraison plus rapide de données de haute qualité.
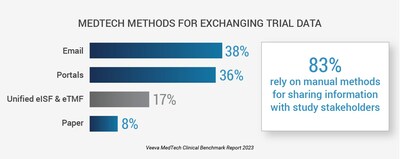
La recherche révèle que la plupart des entreprises de medtech (83 %) utilisent des approches manuelles pour partager l'information avec les intervenants de l'étude, comme les e-mails, les portails et le papier. Les méthodes manuelles de partage de l'information ralentissent l'exécution des études et l'analyse des données, augmentant ainsi le temps et les coûts nécessaires à la réalisation des activités d'essai. Comme les règlements MDR et IVDR de l'UE exigent davantage de preuves cliniques et de données sur la performance, il y a une occasion à court terme de faire progresser les études sur les medtech pour être plus rapides et plus efficaces.
Le rapport met en lumière les principaux domaines à améliorer et les progrès réalisés en matière de recherche clinique réalisée par les medtech, notamment :
- Les systèmes déconnectés demeurent un enjeu crucial : Plus de la moitié des répondants (61 %) rencontrent des difficultés avec les systèmes cliniques fragmentés en raison de l'intégration entre les systèmes, de la gestion des données, des rapports et de l'ergonomie. Gérer des études dans des systèmes cloisonnés peut entraîner des erreurs manuelles, de la duplication de données et des fichiers manquants.
- Une stratégie claire est nécessaire pour le suivi clinique post-commercialisation (PMCF) : La plupart des répondants n'utilisaient pas de méthode unique pour le PCMF, les meilleures approches rapportées étant les données réelles probantes (21 %), les recherches documentaires (20 %) et les études comparatives (20 %). En l'absence d'une méthode normalisée pour assurer le PMCF, les organisations peuvent bénéficier de l'élaboration d'un processus de bout en bout qui couvre les aspects cliniques, médicaux, réglementaires, de qualité et de commercialisation pour la collecte continue de données tout au long du cycle de vie du produit.
- Le passage aux systèmes cliniques numériques s'accélère cette année : Près de la moitié (45 %) affirment que le passage aux systèmes cliniques numériques est une priorité absolue pour les 12 prochains mois. L'établissement d'une base technologique numérique et connectée facilitera la collaboration entre les intervenants de l'étude, augmentera l'efficacité des essais, accélérera la livraison des données et améliorera l'expérience des sites.
« L'industrie des medtech a une occasion importante de moderniser les systèmes et processus cliniques pour un accès plus rapide aux données des essais, a déclaré Kevin Liang, vice-président responsable de la stratégie Vault Clinical, Veeva MedTech. Alors que davantage d'organisations accordent la priorité aux technologies cliniques numériques, les medtech peuvent améliorer la collaboration avec les intervenants et stimuler l'efficacité, la productivité et la conformité des essais. »
L'étude de référence clinique de Veeva MedTech a examiné la façon dont les organisations – des entreprises émergentes aux grandes entreprises de diagnostic et de dispositifs – gèrent les processus cliniques, la collaboration avec le site d'étude et les données d'essai pour assurer la conformité et la rapidité. Ce rapport présente les idées de plus de 135 professionnels de la medtech clinique du monde entier, en décrivant les défis actuels et les priorités à court terme associées à la conduite des essais cliniques. Voir le rapport complet, qui étudie comment les entreprises de medtech gèrent les opérations cliniques, l'externalisation, le suivi clinique post-commercialisation et la modernisation.
À propos de Veeva Systems
Veeva est le leader mondial des logiciels cloud pour le secteur des sciences de la vie. Engagée dans l'innovation, l'excellence des produits et la réussite de ses clients, Veeva compte plus de 1 000 clients, des plus grandes sociétés pharmaceutiques du monde aux nouvelles sociétés de biotechnologie. En tant que société d'intérêt public, Veeva s'engage à équilibrer les intérêts de toutes les parties prenantes, y compris les clients, les employés, les actionnaires et les industries qu'elle sert. Pour plus d'informations, rendez-vous sur veeva.com/eu.
Contact : | |
Jeremy Whittaker Veeva Systems +49-695-095-5486 | Deivis Mercado Veeva Systems 925-226-8821 |

Logo - https://mma.prnewswire.com/media/1488285/Veeva_Systems_Logo.jpg
![]() View original content:https://www.prnewswire.com/news-releases/le-rapport-sur-les-essais-cliniques-de-veeva-medtech-signale-une-occasion-importante-dameliorer-la-distribution-et-la-qualite-des-donnees-301802952.html
View original content:https://www.prnewswire.com/news-releases/le-rapport-sur-les-essais-cliniques-de-veeva-medtech-signale-une-occasion-importante-dameliorer-la-distribution-et-la-qualite-des-donnees-301802952.html
